
根据相关的规定,企业想要开办第二类、第三类医疗器械生产相关活动,应当向所在地省、自治区、直辖市食品药品监督管理部门申请生产许可,第一类医疗器械生产企业需要办理备案。
那么,医疗器械生产许可证如何办理呢?具体需要什么条件呢?
医疗器械生产许可证办理所需材料
(一)《医疗器械生产企业开办申请表》(原件)(包含委托书及被委托人身份证复印件, 以及申请材料真实性的保证声明)。
(二)营业执照复印件;
(三)申请企业持有的所生产医疗器械的注册证及产品技术要求复印件;
(四)法定代表人、企业负责人身份证明复印件;企业负责人任命文件的复印件;
(五)生产、质量和技术部门负责人的身份、学历、职称证明复印件和工作简历(复印件);
(六)拟生产产品范围、品种和相关产品简介。产品简介至少包括对产品的结构组成、原理、预期用途的说明及产品标准生产管理、质量检验岗位从业人员学历、职称一览表;
(七)生产场地的证明文件,有特殊生产环境要求的还应当提交设施、环境的证明文件复印件;一般包含房屋产权证明或租赁协议及出租方房产证明复印件、厂区总平面图、主要生产车间平面图
(八)主要生产设备和检验仪器清单(原件);
(九)质量手册和程序文件(原件);
(十)工艺流程图(原件);
(十一)生产企业自查表(原件);
(十一)其他证明资料(依据各地药监局的具体规定准备);
医疗器械生产许可证办理条件
一、开办第一类医疗器械生产许可证的企业,应当具备与所生产产品相适应的生产条件,并应当在领取营业执照后30日内,填写第一类医疗器械生产企业登记表,并向所在地省、自治区、直辖市(食品)药品监督管理部门书面告知。
二、开办第二类、第三类医疗器械生产许可证的企业,应当满足下列要求:
1. 企业的生产、质量和技术负责人应当具有与所生产医疗器械相适应的专业能力,并掌握国家有关医疗器械监督管理的法律、法规和规章以及相关产品质量、技术的规定。质量负责人不得同时兼任生产负责人;
2. 企业内初级以上职称或者中专以上学历的技术人员占职工总数的比例应当与所生产产品的要求相适应;
3. 企业应当具有与所生产产品及生产规模相适应的生产设备,生产、仓储场地和环境。企业生产对环境和设备等有特殊要求的医疗器械的,应当符合国家标准、行业标准和国家有关规定;
4. 企业应当设立质量检验机构,并具备与所生产品种和生产规模相适应的质量检验能力;
5. 企业应当保存与医疗器械生产和经营有关的法律、法规、规章和有关技术标准。
医疗器械生产许可证办理流程图
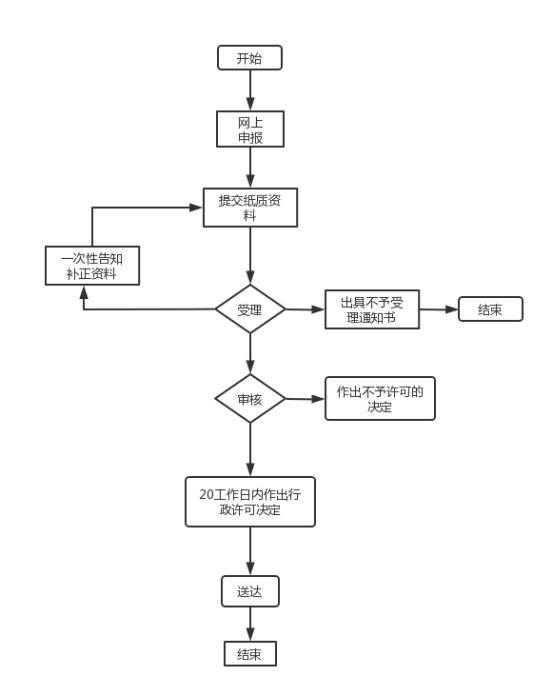
另外值得注意的是,医疗器械生产许可证有效期为五年,在有效期届满前6个月需提出延续申请。

中科智雅医疗技术集团是一家专注于为大健康领域提供产品注册,生产质量管理体系,临床试验研究与技术输出全过程的专业服务机构。专业代办(械、健、食、妆、消)产品注册,体系辅导,生产许可注册服务。
公司被评为中国医疗器械行业协会会员单位,山东省医疗器械行业协会会员,深圳市医疗器械行业协会会员。拥有良好的医疗器械临床试验机构合作平台,畅通的CMDE咨询服务渠道及优秀的数据管理统计团队。公司团队稳定、经验丰富,医学相关专业本硕以上学历人员超过90%,公司先后为国内企业成功提供了千余项专业技术服务,协助(械、健、食、妆、消)企业取得数百张产品注册证,其中II、III类医疗器械注册证,IVD试剂产品注册证,软件类产品注册证600多项。
中科智雅医疗秉承:以服务为先、以技术为重的核心价值观,专一的方向、专业的团队、专注的态 度获得广大医疗器械企业的一致认可。
联系方式|400-877-6069
公司地址|山东省济南市槐荫区西进时代中心B座1014室
|
上一条:医疗器械注册证有效期几年?注册证到期怎么办?
下一条:江苏发布医疗器械生产分级监管实施办法,4月7日起施行! |
返回列表 |